СЕЛЕНОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ, вещества, содержащие в молекуле связь
углерод - селен. Главные типы С. с. (R, Аr - органич. остаток): селениды R2Se,
диселениды RSe-SeR, селенолы RSeH, селеноксиды R2SeO, селеноны R2SeO2,
селениновые к-ты RSeO2H, ceленоновые к-ты RSeO3H,
селенониевые соли R2Se+X- (Х- -
анион, напр. С1-), алкил(арил)селенгалогениды R2SeX2
и RSeX3 (X - атом галогена), селенистые гетероциклы, напр, селенофен.
Основные методы получения С. с.
1. Взаимодействие алкилгалогенидов (1) или арилдиазонийгалогенидов (2) с Na2Se:
2RX + Na2Se->R2Se
+ 2NaX (1)
ArN2X + Na2Se
-> Ar2Se + 2NaX + N2 (2)
2. Взаимодействие металлоорганич. соединений с Se или SeO2:
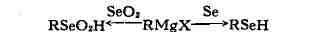
3. Селенирование ароматич. соединений:
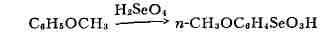
Селенофен (I) получают взаимодействием бутадиена с SеO2 или Se,
напр.:
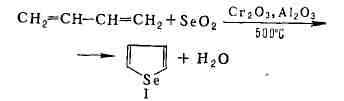
По хим. свойствам С. с. аналогичны сераорганическим соединениям; вследствие
усиления металлич. свойств у селена по сравнению с серой связь С-Se
расщепляется галогенами и окислителями легче, чем связь С-S. Селеноновые к-ты -
сильные окислители. Практич. значение имеют производные селенофена.
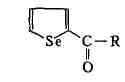
Селеноилацетон (R = СН3) и селеноилтрифторацетон (R = CF3)
образуют хелатные комплексы с ионами металлов (Си, Th, Zr, Hf) и применяются
для экстракционного разделения и выделения элементов.