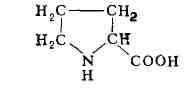
ПРОЛИН, а-пирролидинкарбоновая к-та; гетероциклич. аминокислота (точнее
иминокислота); существует в оптически-активных D- и L- и рацемической
DL-формах. Вторичная аминогруппа П. обусловливает его необычную нингидриновую
реакцию (оранжевая окраска вместо сине-фиолетовой).
L-П. содержится во всех природных белках. Особенно богаты им растительные
белки - проламины, белки соединительной ткани (10-15% в коллагене),
В-казеин. L-П. входит в состав инсулина, адрено-кортикотропного гормона,
грамицидина С и др. биологически важных пептидов. D-П. входит в состав нек-рых алкалоидов.
Гидролиз пептидных связей входящего в пептиды L-П. катализируют
ферменты пролиназа (связь по СО-группе) и пролидаза (связь по NH-группе). П.-
заменимая аминокислота; её биосинтез в живом организме протекает через
у-полуальдегид глутаминовой кислоты или из орнитина. Окислением с
участием аскорбиновой к-ты П. превращается в оксипролин. DL-П.
синтезирован в 1900 Р. Вильштеттером и выделен вместе с L-П. в 1901 из
гидролизата казеина Э. Фишером.