БРОЖЕНИЕ, процесс анаэробного расщепления органических веществ, преим. углеводов, происходящий под влиянием микроорганизмов или выделенных из них ферментов.
В ходе Б. в результате сопряжённых окислительно-восстановит. реакций
освобождается энергия, необходимая для жизнедеятельности микроорганизмов, и
образуются химич. соединения, к-рые микроорганизмы используют для биосинтеза
аминокислот, белков, ор-ганич. к-т, жиров и др. компонентов тела. Одновременно
накапливаются конечные продукты Б. В зависимости от их характера различают Б.
спиртовое, молочнокислое, маслянокислое, пропионовокис-лое, ацетоно-бутиловое,
ацетоно-этиловое и др. виды. Характер Б., его интенсивность, количественные соотношения
конечных продуктов, а также направление Б. зависят от особенностей его
возбудителя и условий, при к-рых Б. протекает (рН, аэрация, субстрат и др.).
Спиртовое Б. В 1836 франц. учёный Каньяр де ла Тур установил, что спиртовое
Б. связано с ростом и размножением дрожжей. Химич. уравнение спиртового Б.: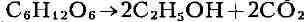
было дано франц. химиками А. Лавуазье (1789) и Ж. Гей-Люссаком (1815).
Л. Пастер пришёл к выводу (1857), что спиртовое Б. могут вызывать только
живые дрожжи в анаэробных условиях ("Брожение - это жизнь без
воздуха"). В противовес этому нем. учёный Ю. Ли-бих упорно
настаивал на том, что Б. происходит вне живой клетки.
На возможность бесклеточного спиртового Б. впервые (1871) указала
рус. врач-биохимик М. М. Манассеина. Нем. химик Э. Бухнер в 1897, отжав под
большим давлением дрожжи, растёртые с кварцевым песком, получил бесклеточный
сок, сбраживаю-щий сахар с образованием спирта и СО2. При нагревании
до 500С и выше сок утрачивал бродильные свойства. Всё это указывало
на ферментативную природу активного начала, содержащегося в дрожжевом соке.
Рус. химик Л. А. Иванов обнаружил (1905), что добавленные к дрожжевому
соку фосфаты в неск. раз повышают скорость Б. Исследования отечеств, биохимиков
А. Н. Лебедева, С. П. Костычева, Я. О. Парнаса и нем. биохимиков К. Нейберга,
Г. Эмбдена, О. Мейергофа и др. подтвердили, что фосфорная к-та участвует в важнейших
этапах спиртового Б.
В дальнейшем мн. исследователи детально изучили ферментативную природу и
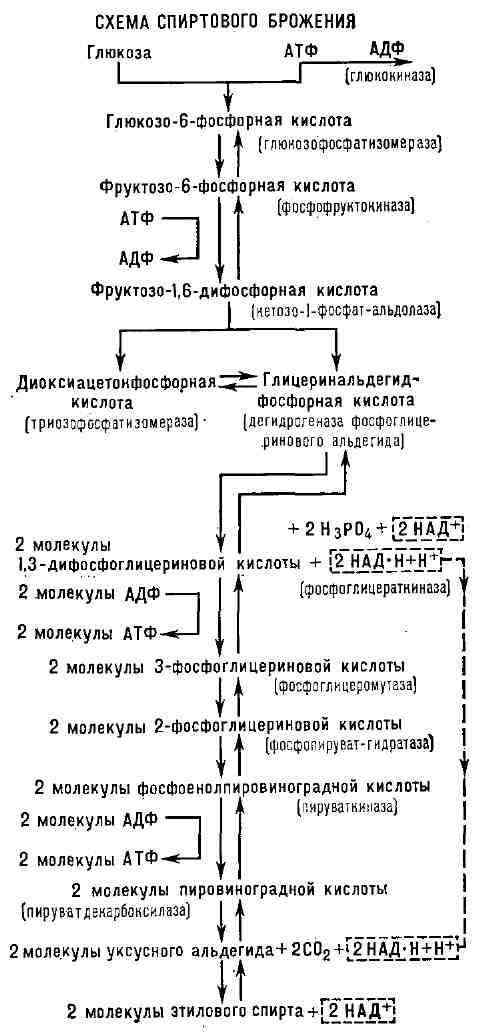
механизм спиртового Б. (см. схему).
Первая реакция превращения глюкозы при спиртовом Б.- присоединение к глюкозе
под влиянием фермента глюкокина-зы остатка фосфорной к-ты от
аденозин-трифосфорной к-ты (АТФ, см. Аденозин-фосфорные кислоты). При
этом образуются аденозиндифосфорная к-та (АДФ) и глюкозо-6-фосфорная к-та.
Последняя под действием фермента глюкозофосфати-зомеразы превращается в
фруктозо-6-фос-форную к-ту, к-рая, получая от новой молекулы АТФ (при участии
фермента фосфофруктокиназы) ещё один остаток фосфорной к-ты, превращается в
фрукто-зо-1,6-дифосфорную к-ту. (Эта и следующая реакции, обозначенные
встречными стрелками, обратимы, т. е. их направление зависит от условий -
концентрации фермента, рН и др.) Под влиянием фермента
кетозо-1-фосфат-альдолазы фрук-тозо-1,6-дифосфорная к-та расщепляется на
глицеринальдегидфосфорную и ди-оксиацетонфосфорную к-ты, к-рые могут
превращаться друг в друга под действием фермента триозофосфатизомера-зы.
Глицеринальдегидфосфорная к-та, присоединяя молекулу неорганич. фосфорной к-ты
и окисляясь под действием фермента дегидрогеназы фосфоглицерин-альдегида,
активной группой к-рого у дрожжей является никотинамидадеыин-динуклеотид (НАД),
превращается в 1,3-дифосфоглицериновую к-ту. Молекула диоксиацетонфосфорной
к-ты под действием триозофосфатизомеразы даёт вторую молекулу
глицеринальдегид-фосфорной к-ты, также подвергающуюся окислению до
1,3-дифосфоглицериновой к-ты; последняя, отдавая АДФ (под действием фермента
фосфоглицераткиназы) один остаток фосфорной к-ты, превращается в
3-фосфоглицериновую к-ту, к-рая под действием фермента фосфоглицеро-мутазы
превращается в 2-фосфоглицери-новую к-ту, а она под влиянием фермента фосфопируват-гидратазы
- в фосфоенол-пировиноградную к-ту. Последняя при участии фермента
пируваткиназы передаёт остаток фосфорной к-ты молекуле АДФ, в результате чего
образуется молекула АТФ и молекула енолпировиноград-ной к-ты, к-рая весьма
нестойка и переходит в пировиноградную к-ту. Эта к-та при участии имеющегося в
дрожжах фермента пируватдскарбоксилазы расщепляется на уксусный альдегид и
двуокись углерода. Уксусный альдегид, реагируя с образовавшейся при окислении
глице-ринальдегидфосфорной к-ты восстановленной формой
никотинамидаденинди-нуклеотида (НАД*Н), при участии фермента
алкогольдегидрогеназы превращается в этиловый спирт.
Суммарно уравнение спиртового Б. может быть представлено в след, виде:
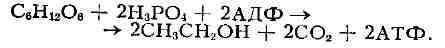
Т. о., при сбраживании 1 моля глюкозы образуются 2 моля этилового
спирта, 2 моля СО2, а также в результате фос-форилирования 2 молей
АДФ образуются 2 моля АТФ. Термодинамич. расчёты показывают,
что при спиртовом Б. превращение 1 моля глюкозы может сопровождаться
уменьшением свободной энергии примерно на 210 кдж (50 000 кал),
т. е. энергия, аккумулированная в 1 моле этилового спирта, на 210 кдж
(50 000 кал) меньше энергии 1 моля глюкозы. При
образовании 1 моля АТФ (макроэргических - богатых энергией
фосфатных соединений) используется 42 кдж (10 000 кал). Следовательно,
значит, часть энергии, освобождающейся при спиртовом Б., запасается в виде АТФ,
обеспечивающей разнообразные энергетич. потребности дрожжевых клеток. Такое же
биологич. значение имеет процесс Б. и у др. микроорганизмов. При полном
сгорании 1 моля глюкозы (с образованием СО2 и Н2О)
изменение свободной энергии достигает 2,87 Мдж (686 000 кал). Иначе
говоря, дрожжевая клетка использует лишь 7% энергии глюкозы. Это показывает малую
эффективность анаэробных процессов по сравнению с процессами, идущими в
присутствии кислорода. При наличии кислорода спиртовое Б. угнетается или
прекращается и дрожжи получают энергию для жизнедеятельности в процессе
дыхания. Наблюдается тесная связь между Б. и дыханием микроорганизмов, растений
и животных. Ферменты, участвующие в спиртовом Б., имеются также в тканях
животных и растений. Во мн. случаях первые этапы расщепления Сахаров, вплоть до
образования пировиноградной к-ты,- общие для Б. и дыхания. Большое значение
процесс анаэробного распада глюкозы имеет и при сокращении мышц (см. Гликолиз),
первые этапы этого процесса также сходны с начальными реакциями спиртового
Б.
Сбраживание углеводов (глюкозы, ферментативных гидролизатов крахмала,
кислотных гидролизатов древесины) используется во многих отраслях
промышленности: для получения этилового спирта, глицерина и др. технических и
пищевых продуктов. На спиртовом Б. основаны приготовление теста в хлебопекарной
промышленности, виноделие и пивоварение.
Молочнокислое Б. Молочнокислые бактерии подразделяют на 2 группы -
гомоферментативные и гетероферментативные. Гомоферментативные бактерии (напр.,
Lactobacillus delbruckii) расщепляют моносахариды с образованием двух
молекул молочной к-ты в соответствии с суммарным уравнением:
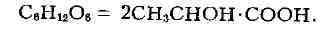
Гетероферментативные бактерии (напр., Bacterium lactis aerogenes) ведут
сбра-живание с образованием молочной к-ты, уксусной к-ты, этилового спирта и СО2,
а также образуют небольшое кол-во ароматич. веществ - диацетила, эфиров и т. д.
При молочнокислом Б. превращение углеводов, особенно на первых этапах,
близко к реакциям спиртового Б., за исключением декарбоксилирования
пировиноградной к-ты, к-рая восстанавливается до молочной к-ты за счёт
водорода, получаемого от НАД*Н. Гомофермен-тативное молочнокислое Б.
используется для получения молочной к-ты, при изготовлении различных кислых
молочных продуктов, хлеба и в силосовании кормов в с. х-ве.
Гетероферментативное молочнокислое Б. происходит при консервировании различных
плодов и овощей путём квашения.
Маслянокислое Б. Сбраживание углеводов с преим. образованием масляной к-ты
производят мн. анаэробные бактерии, относящиеся к роду Clost-ridium. Первые
этапы расщепления углеводов при маслянокислом Б. аналогичны соответств. этапам
спиртового Б., вплоть до образования пировиноградной к-ты, из к-рой при
маслянокислом Б. образуется ацетил-кофермент А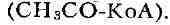 Ацетил-КоА может служить предшественником масляной к-ты, подвергаясь следующим
превращениям:
Ацетил-КоА может служить предшественником масляной к-ты, подвергаясь следующим
превращениям:
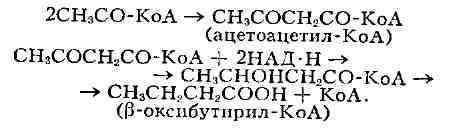
Маслянокислое Б. применялось для получения масляной к-ты из крахмала.
Ацетоно-бутиловое Б. Бактерии Clostridium acetobutylicum сбра-живают
углеводы с преим. образованием бутилового спирта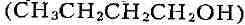 и
ацетона
и
ацетона 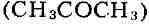 . При этом образуются также в сравнительно небольших кол-вах водород, СО2,
уксусная, масляная к-ты, этиловый спирт. Первые этапы расщепления углеводов те
же, что и при спиртовом Б. Бутиловый спирт образуется путём восстановления
масляной к-ты:
. При этом образуются также в сравнительно небольших кол-вах водород, СО2,
уксусная, масляная к-ты, этиловый спирт. Первые этапы расщепления углеводов те
же, что и при спиртовом Б. Бутиловый спирт образуется путём восстановления
масляной к-ты:
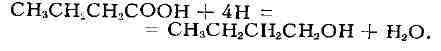
Ацетон же образуется декарбоксилированием ацетоуксусной к-ты, к-рая
получается в результате конденсации двух молекул уксусной к-ты. Исследованиями
В. Н. Шапошникова показано, что ацетоно-бутиловое Б. (как и ряд др., напр,
пропионовокислое, Маслянокислое) в опытах с растущей культурой
происходит в две фазы. В первую фазу Б. параллельно с нарастанием биомассы
накапливаются уксусная и масляная к-ты; во вторую фазу образуются преим. ацетон
и бутиловый спирт. При ацетоно-бутиловом Б. сбраживаются моносахариды,
дисаха-риды и полисахариды - крахмал, инсулин, но не сбраживаются клетчатка и
гемицеллюлоза. Ацетоно-бутиловое Б. использовалось для пром. получения
бутилового спирта и ацетона, применяемых в химич. и лакокрасочной пром-сти (см.
также Ацетоно-бутиловое брожение и Ацетоно-этиловое брожение).
Сбраживание белков. Некоторые бактерии из рода Clostridium - гнилостные анаэробы
- способны сбраживать не только углеводы, но и аминокислоты. Эти бактерии
более приспособлены к использованию белков, расщепляемых ими при помощи
протеолитических ферментов до аминокислот, к-рые затем подвергаются Б. Процесс
сбраживания белков имеет значение в круговороте веществ в природе (см. Гниение).
Пропионовокислое Б. Осн. продукты пропионовокислого Б., вызываемого
несколькими видами бактерий из рода Propionibacterium,- пропионовая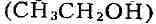 и уксусная к-ты и
и уксусная к-ты и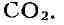
Химизм пропионовокислого Б. сильно изменяется в зависимости от условий. Это,
по-видимому, объясняется способностью пропионовых бактерий перестраивать обмен
веществ, напр. в зависимости от аэрации. При доступе кислорода они ведут
окислительный процесс, а в его отсутствии расщепляют гексозы путём Б. Пропионовые
бактерии способны фиксировать СО2, при этом из пировиноградной к-ты
и СО2 образуется щавелевоуксусная к-та, превращающаяся в янтарную
к-ту, из к-рой декарбоксилированием образуется пропионовая к-та:
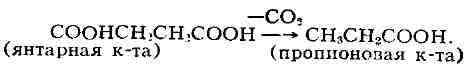
Существуют Б., к-рые сопровождаются и восстановительными процессами.
Примером такого "окислительного" Б. служит лимоннокислое Б. Мн.
плесневые грибы сбраживают сахара с образованием лимонной к-ты. Наиболее
активные штаммы Aspergillus niger превращают до 90% потреблённого сахара в
лимонную к-ту. Значит, часть лимонной к-ты, используемой в пищ.
пром-сти, производится микробиол. путём - глубинным и поверхностным
культивированием плесневых грибов.
Иногда по традиции и чисто окислительные процессы, осуществляемые
микроорганизмами, паз. Б. Примерами таких процессов могут служить уксуснокислое
и глюконовокислое Б.
Уксуснокислое Б. Бактерии, относящиеся к роду Acetobacter, окисляют этиловый
спирт в уксусную к-ту в соответствии с суммарной реакцией:
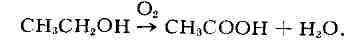
Промежуточное соединение при окислении спирта в уксусную к-ту - уксусный
альдегид. Мн. уксуснокислые бактерии, кроме окисления спирта в уксусную к-ту,
осуществляют окисление глюкозы в глю-коновую и кетоглюконовую к-ты.
ГлюконовокислоеБ. осуществляют и нек-рые плесневые грибы, способные окислять
альдегидную группу глюкозы, превращая последнюю в глю-коновую к-ту:
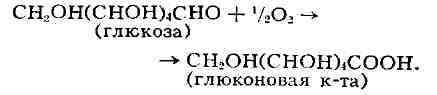
Кальциевая соль глюконовой к-ты Служит хорошим источником кальция для людей
и животных.
Лит.: Шапошников В. Н-, Техническая микробиология, М., 1948; Прескот
С., Дэн С., Техническая микробиология, пер. с англ.. М-, 1952; Пастер Л., Избр.
труды, пер. с франц., т. 1 - 2, М., 1960; Кретович В. Л., Основы биохимии
растений, 4 изд., М., 1964; Фробишер М., Основы микробиологии, пер. с англ.,
М.,.1965; Фердман Д. Л., Биохимия, М., 1966; Работнова И. Л., Общая
микробиология. М., 1966. В.И.Любимов.
БРОЙЛЕР (англ, broiler, от broil - жарить на огне), мясной цыплёнок в
возрасте 60 сут (живая масса 1,4-1,6 кг). Мясо нежное, сочное, с
небольшим количеством жира, диетич. свойства выше, чем у взрослой птицы. Для
произ-ва Б. в основном используют мясо-яичные и мясные породы кур и
специализированные мясные линии этих пород. Наиболее выгодны помеси от
скрещивания мясных линий, селекционированных по скорости роста, быстроте
оперяемости, мясным формам и высокой оплате корма. Произ-во Б. наиболее выгодно
в крупных специализированных х-вах. Технологич. процесс на бройлерной ф-ке
начинается на ферме-репродукторе, Где проводится скрещивание линий и
организуется круглогодовое произ-во гибридных яиц для инкубации. Из цеха
инкубации суточный молодняк поступает в цех выращивания Б. и частично в цех
выращивания "ремонтного" молодняка. Выращивают Б. в безвыгульных
широкогабаритных механизированных птичниках на глубокой подстилке или в
клетках. Кормят сухими комбикормами. Забивают Б. в цехе переработки.
Производств, мощности цехов рассчитаны на поточную систему произ-ва и
равномерный во все сезоны года выпуск продукции. Бройлерная пром-сть развита в
США, Англии, ГДР, ФРГ, Чехословакии, Венгрии, Бельгии и др. странах. В СССР
созданы бройлерные ф-ки производительностью 2-3 млн. Б. в год: совхоз
"Красный" в Крымской обл., Березовская в Красноярском крае, Загорская
в Московской обл. и др. Лит.: Богданов М. Н., ИофеН. Ш., Выращивание
мясных цыплят, М., 1961; Производство бройлеров за рубежом, М., 1962; Терещенко
В. И., Экономика и организация производства бройлеров в США, Киев, 1965; Белов
Л. М., М а рч и к В. Ф., Тютюнников В. Н., Производство бройлеров в совхозе
"Красный", М., 1966. С. И. Сметнев.
БРОЙЛЬ, де Брольи (de Broglie) Луи де (р. 15. 8. 1892, Дьеп),
французский физик. Член (1933) и непременный секретарь (1942) Франц. АН.
Иностранный член АН СССР (1958). Окончил Парижский ун-т (1909). С 1928
преподавал там же. В 1924 в докторской дисс. "Исследования по теории
квантов" выдвинул идею о волновых свойствах материи (т. н. волны де
Бройля), к-рая легла в основу совр. квантовой механики. Волновые свойства
микрочастиц были подтверждены впоследствии опытами по дифракции электронов и
др. частиц. Б. занимался также релятивистской квантовой механикой, вопросами
строения ядра, теорией распространения электромагнитных волн в волноводах. Б.
принадлежат также работы по истории физики. Нобелевская пр. (1929). Соч. :
Recherchessurlatheoriedequanta, "Annalesdephysique", 1925, t. 3, № 1;
Delamecaniqueondulatoirealatheoriedunoyau, t. 1 - 2, P., 1943 - 45; в рус. пер.
- Введение в волновую механику, Хар. - К., 1934; Магнитный электрон, Хар.,
1936; Электромагнитные волны в волноводах и полых резонаторах, М., 1948;
Революция в физике (Новая физика и кванты), М., 1965. Лит.: Louis de Broglie. Physicien et pen-seur, P.,
1953 (имеетсябибл. трудовБ. ).
БРОКА (Вгоса) Поль (28. 6. 1824, Сент-Фуа-ла-Гранд,- 9. 7. 1880,
Париж), французский анатом и антрополог, один из основателей совр. антропологии,
инициатор создания в Париже Антропологич. науч. об-ва (1859). Осн. работы
по сравнит, анатомии приматов, вопросам общей антропологии, расовым типам совр.
и древнего населения Франции. Разработал первое в мире руководство по антропометрии
и краниометрии (1865); построил шкалы для определения окраски глаз, волос и
кожи; изобрёл ряд антропометрич. инструментов. Соч. : Общие инструкции для
антропологических исследований и наблюдений, [пер. -с франц. ], в сб. :
Известия Императорского общества любителей естествознания, антропологии и
этнографии, т. 2, М., 1865; Instructions craniologiques et craniometriques de
la Sosiete d'Anthropologie de Paris redigees. P., 1875. Т. Д. Гладкова.
БРОКГАУЗ, Брокхауз (Brockhaus), немецкая издательская фирма. Осн. Ф.
А. Брокгаузом (1772-1823) в 1805 в Амстердаме, в 1811-17 находилась в
Альтенбурге, а затем перебазирована в Лейпциг. С 1808 издавала энциклопедию
"Conversations Lexikon", широко известную под назв.
"Брокгауз" (в 19 в. вышло 14 изданий; 15-е и 16-е издания
энциклопедии выпущены под назв. ^Большой Брокгауз*), и ряд др. изданий.
После образования ГДР Б. в Лейпциге - народное издательство (с 1953); выпускает
географич. и этнографич. лит-ру и справочные издания. В ФРГ фирма Б.
обосновалась в Висбадене; в 1952-57 ею был издан новый 12-томный "Большой
Брокгауз" ("Der Grosse Brockhaus"), в 1962-63 - 2 дополнит, тома
к нему ("Erganzungsbande"), в 1958-60 - 5-томный "Новый
Брокгауз" ("Der Neue Brockhaus"), в 1964 - дополнит, том к нему
("Erganzungsband"), в 1961-62 - 2-томный "Малый Брокгауз"
("Der Kleine Brockhaus"), в 1959 - "Народный Брокгауз"
("Der Volks-Brockhaus", 2 изд. ). С 1966 выпускается 20-томное 17-е
издание "Brockhaus Enzyklopadie" (Bd 1-10-, Wiesbaden).
БРОКГАУЗА И ЕФРОНА ЭНЦИКЛОПЕДИЧЕСКИЙ СЛОВАРЬ, крупнейшая дореволюционная
русская универсальная энциклопедия, выпущенная акционерным издательским
обществом Ф. А. Брокгауз - И. А. Ефрон. Состоит из 86 тт. (82 основных и 4
дополнительных), выходивших в течение 1890-1907. Первые 8 томов вышли под общей
ред. И. Е. Андреевского, все последующие - под ред. К. К. Арсеньева и Ф. Ф.
Петрушевского. К созданию словаря были привлечены крупнейшие научные силы того
времени: Д. И. Менделеев, А. И. Бекетов, А. И. Воейков, Д. И. Анучин, Ю. М.
Шокальский, Н. М. Книпович, А. О. Ковалевский, А. И. Советов и др. Как и все
рус. энциклопедии дореволюционного времени, Б. и Е. э. с. не отличается
единством идеологич. принципов. В условиях старой России осуществление такого
большого и сложного по составу издания, как многотомная универсальная энциклопедия,
было возможно только на путях более или менее тесного сотрудничества
представителей различных мировоззрений (так, напр., раздел философии возглавлял
философ-идеалист В. С. Соловьёв). Однако большая насыщенность словаря фактич.
материалом, обилие библиографич. сведений сохраняют за ним значение важного
справочного издания. С 1911 то же изд-во стало выпускать Новый
энциклопедический словарь под ред. К. К. Арсеньева, рассчитанный на более
широкие круги читателей. Издание осталось незаконченным: из намеченных 48 тт.
вышли в течение 1911 -16 29 томов (последнее слово - "Отто"). Лит.:
Кауфман И. М-, Русские энциклопедии, в. 1, М., 1960. И. М. Кауфман.
БРОКДОРФ-РАНЦАУ (Brockdorff-Rantzau) Ульрих (29. 5. 1869, Шлезвиг,-
8. 9. 1928, Берлин), граф, германский дипломат. В 1912-18 посланник в Дании.
После Ноябрьской революции 1918 в Германии статс-секретарь иностр. дел. В февр.
- июне 1919 мин. иностр. дел в правительстве Ф. Шейдемана. В июне 1919, будучи
пред. герм, делегации на Парижской мирной конференции, возражал против принятия
Германией условий Версальского мирного договора. После решения Веймарского
учредит, собрания о подписании договора вышел в отставку. В 1922-28 посол в
СССР. Был сторонником установления дружеств. отношений между Германией и СССР и
развития между ними экономич. связей.
БРОКЕН-ХИЛЛ (Broken Hill, от broken - разбитый и hill - холм), город
в Австралийском Союзе, в шт. Новый Юж. Уэльс. 30,3 тыс. жит. (1968). Важный
горнопром. центр страны, возникший в 1883-84 в связи с разработками месторождений
полиметаллич. руд. Добыча свинца и цинка. Концентрат свинца вывозится для
черновой плавки в Порт-Пири, с к-рым Б. связан жел. дорогой.
БРОКЕН-ХИЛЛ (совр. назв. Кабве), город в Замбии, в районе
к-рого в 1921 были открыты костные остатки ископаемого человека. Обнаружен
крупный череп, отличающийся примитивными особенностями (мощный надглазничный
валик, убегающий назад лоб, массивная лицевая часть). Объём мозга небольшой
(1280 ел3). Человека из Б. (др. назв. - "родезийский
человек") относят к палеоантропам, хотя нек-рые признаки сближают
его с питекантропами. Предполагают, что человек из Б. жил довольно
поздно и, может быть, одновременно с ранними представителями позднепалеолитич.
людей совр. физич. типа. Большинство учёных считает его боковой формой в
эволюции человека. Лит.: Нестурх М. Ф., Происхождение человека, М.,
1958; Рогинский Я. Я., Внеевропейские палеоантропы, в кн. : Ископаемые гоминиды
и происхождение человека, М., 1966 (библ. ).
БРОКЕР (англ, broker), посредник при заключении различных сделок; см.
также Посредничество биржевое.
БРОККЕЛЬМАН, Брокельман (Brockelmann) Карл (17. 9. 1868, Росток,- 6.
5. 1956, Галле), немецкий востоковед. Работал в области истории Востока,
истории араб, лит-ры, семитологии. С 1900 проф. ун-тов Бреслау, Кенигсберга,
Галле, Берлина, в 1923-36 - Бреслау, с 1946 - Галле (ГДР). Важнейшее соч. Б. -
библиографич. справочник "История арабской литературы" (т. 1-2, 1898
- 1902) - свод материалов об араб, и арабоязычных поэтах, литераторах, учёных,
об их соч. с 6 по 20 вв. Большой фактич. материал содержит также "История
мусульманских народов и 'государств" (1939). Соч. : Geschichte der arabischen Littera-tur, 2
Aufl., Bd 1 - 2, Leiden, 1943 - 49; Supplementbande 1 - 3, Leiden, 1937-42;
Arabische Grammatik, 16 Aufl., Lpz., 1965; Syrische Grammatik, Lpz., 1965;
Geschichte der islamischen Volker und Staaten, Munch. - В., 1939. Лит.: К р а ч
к о в с к и и И. Ю., Избр. соч., т. ' 2, М. -. Л., 1956, с.. 543-47; Spies О., Verzeichnis der Schriften von Carl
Brockelmann, Lpz., 1938. Л. де Бройль. В. Броневский.
БРОККЕН (Brocken), вершина в ГДР, наиболее высокая в горах Гарц,- 1142
м. Сложена гранитом, имеет форму усечённого конуса. Туризм. С Б. связан
ряд герм. нар. легенд (шабаш ведьм на Б. в Вальпургиеву ночь и др. ).
БРОККОЛИ, спаржевая капуста (Brassica cauliflora subsp. simplex),
однолетнее овощное растение сем. крестоцветных, подвид цветной капусты.
Возделывается в районах с тёплой зимой (в субтропиках). В пищу употребляют
мясистую головку - видоизменённое соцветие. Агротехника такая же, как у цветной
капусты.
БРОКТОН (Brockton), город на С. -В. США, в шт. Массачусетс, в 30 км
от Бостона. 83 тыс. жит., с пригородной зЪной 155 тыс. жит. (1969). Занятых
в пром-сти 16 тыс. Один из старейших центров обувной пром-сти США. Произ-во
обуви (гл. обр. мужской) и машин для сё изготовления.
БРОМ (лат. Bromum), Вг, химич. элемент VII группы периодич.
системы Менделеева, относится к галогенам; ат. н. 35, ат. масса 79,904;
красно-бурая жидкость с сильным неприятным запахом. Б. открыт в 1826 франц.
химиком А. Ж. Баларом при изучении рассолов средиземноморских соляных
промыслов;
назван от греч. bromos - зловоние. Природный Б. состоит из 2 стабильных
изотопов 79Вr (50,54%) и 81Вr (49,46%). Из
искусственно полученных радиоактивных изотопов Б. наиболее интересен 80Вr,
на примере к-рого И. В. Курчатовым открыто явление изомерии атомных
ядер.
Нахождение в природе. Содержание Б. в земной коре (1,6*10-4% по
массе) оценивается в 1015-1016т. В главной своей
массе Б. находится в рассеянном состоянии в магматич. породах, а также в широко
распространённых га-логенидах. Б.- постоянный спутник хлора. Бромистые соли
(NaBr, KBr, MgBr2) встречаются в отложениях хлористых солей (в
поваренной соли до 0,03% Вr, в калийных солях - сильвине и карналлите - до 0.3%
Вr), а также в морской воде (0,065% Вr), рапе соляных озёр (до
0,2% Вr) и подземных рассолах, обычно связанных с соляными и нефтяными
месторождениями (до 0,1% Вr). Благодаря хорошей растворимости в воде
бромистые соли накопляются в остаточных рассолах морских и озёрных водоёмов. Б.
мигрирует в виде легко растворимых соединений, очень редко образуя твёрдые
минеральные формы, представленные бромиритом AgBr, эмболитом Ag (Cl, Вг)
и иодэмболитом Ag (C1, Вr, I). Образование минералов происходит в
зонах окисления сульфидных серебро-содержащих месторождений, формирующихся в
засушливых пустынных областях. См. также Бромиды, природные.
Физические и химические свойства. При - 7,20С жидкий Б.
застывает, превращаясь в красно-коричневые игольчатые кристаллы со слабым металлич.
блеском. Пары Б. жёлто-бурого цвета, tкип 58,780С.
Плотность жидкого Б. (при 200С) 3,1 г/см3.
В воде Б. растворим ограниченно, но лучше других галогенов (3,58 г Б. в
100 г Н2О при 200С). Ниже 5,840С
из воды осаждаются гранатово-красные кристаллы 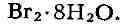 Особенно хорошо растворим Б. во многих органич. растворителях, чем пользуются
для извлечения его из водных растворов. Б. в твёрдом, жидком и газообразном
состоянии состоит из 2-атомных молекул. Заметная диссоциация на атомы
начинается при темп-ре ок. 8000С; диссоциация наблюдается и при
действии света.
Особенно хорошо растворим Б. во многих органич. растворителях, чем пользуются
для извлечения его из водных растворов. Б. в твёрдом, жидком и газообразном
состоянии состоит из 2-атомных молекул. Заметная диссоциация на атомы
начинается при темп-ре ок. 8000С; диссоциация наблюдается и при
действии света.
Конфигурация внешних электронов атома Б. 4s2 4p5.
Валентность Б. в соединениях переменна, степень окисления равна - 1 (в
бромидах, напр. КВr), +1 (в гипобромитах, NaBrO), +3 (в бромитах,
NaBrO2), +5 (в броматах, КВrОз) и + 7 (в перброматах,
NaBrO4). Химически Б. весьма активен, занимая по реакционной
способности место между хлором и иодом. Взаимодействие Б. с серой, селеном,
теллуром, фосфором, мышьяком и сурьмой сопровождается сильным разогреванием,
иногда даже появлением пламени. Так же энергично Б. реагирует с нек-рыми
металлами, напр, калием и алюминием. Однако многие металлы реагируют с
безводным Б. с трудом из-за образования на их поверхности защитной плёнки
бромида, нерастворимого в Б. Из металлов наиболее устойчивы к действию Б., даже
при повышенных темп-pax и в присутствии влаги, серебро, свинец, платина и
тантал (золото, в отличие от платины, энергично реагирует с Б.). С
кислородом, азотом и углеродом Б. непосредственно не соединяется даже при
повышенных темп-pax. Соединения Б. с этими элементами получают косвенным путём.
Таковы крайне непрочные окислы Вr2О, ВrО2 и Вr3О8
(последний получают, напр., действием озона на Б. при 800С).
С галогенами Б. взаимодействует непосредственно, образуя BrF3, BrF5,
BrCl, IBr и др. (см. Межгалогенные соединения).
Б.- сильный окислитель. Так, он окисляет сульфиты и тиосульфаты в водных растворах
до сульфатов, нитриты до нитратов, аммиак до свободного азота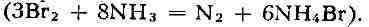 Б. вытесняет иод из его соединений, но сам вытесняется хлором и фтором.
Свободный Б. выделяется из водных растворов бромидов также под действием
сильных окислителей
Б. вытесняет иод из его соединений, но сам вытесняется хлором и фтором.
Свободный Б. выделяется из водных растворов бромидов также под действием
сильных окислителей 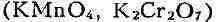 в кислой среде.
в кислой среде. 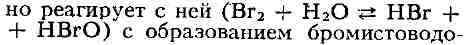 При растворении в воде Б. частич. родной кислоты НВг и неустойчивой бром-новатистой
кислоты НВгО. Раствор Б. в воде наз. бромной водой. При растворении
Б. в растворах щелочей на холоду
При растворении в воде Б. частич. родной кислоты НВг и неустойчивой бром-новатистой
кислоты НВгО. Раствор Б. в воде наз. бромной водой. При растворении
Б. в растворах щелочей на холоду
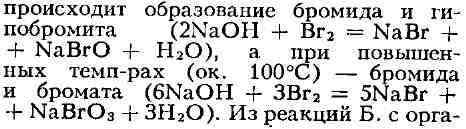 нич.
нич.
соединениями наиболее характерны присоединение по двойной связи С=С, а также
замещение водорода (обычно при действии катализаторов или света).
Получение и применение. Исходным сырьём для получения Б. служат морская вода,
озёрные и подземные рассолы и щелока калийного произ-ва, содержащие Б. в виде
бромид-иона Вr- (от 65 г/м3 в морской воде до 3-4 кг/м3
и выше в щелоках калийного произ-ва). Б. выделяют при помощи
хлора 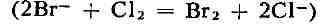 и отгоняют из раствора водяным паром или воздухом. Отгонку паром ведут в
колоннах, изготовленных из гранита, керамики или иного стойкого к Б. материала.
Сверху в колонну подают подогретый рассол, а снизу - хлор и водяной пар. Пары
Б., выходящие из колонны, конденсируют в керамиковых холодильниках. Далее Б.
отделяют от воды и очищают от примеси хлора дистилляцией. Отгонка воздухом
позволяет использовать для получения Б. рассолы с его низким содержанием,
выделять Б. из к-рых паровым способом в результате большого расхода пара
невыгодно. Из получаемой бромовоз душной смеси Б. улавливают химич.
поглотителями. Для этого применяют растворы бромистого железа
и отгоняют из раствора водяным паром или воздухом. Отгонку паром ведут в
колоннах, изготовленных из гранита, керамики или иного стойкого к Б. материала.
Сверху в колонну подают подогретый рассол, а снизу - хлор и водяной пар. Пары
Б., выходящие из колонны, конденсируют в керамиковых холодильниках. Далее Б.
отделяют от воды и очищают от примеси хлора дистилляцией. Отгонка воздухом
позволяет использовать для получения Б. рассолы с его низким содержанием,
выделять Б. из к-рых паровым способом в результате большого расхода пара
невыгодно. Из получаемой бромовоз душной смеси Б. улавливают химич.
поглотителями. Для этого применяют растворы бромистого железа 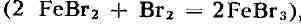 , к-рое, в свою очередь, получают восстановлением FeBr3 железными
стружками, а также растворы гидроокисей или карбонатов натрия или газообразный
сернистый ангидрид, реагирующий с Б. в присутствии паров
, к-рое, в свою очередь, получают восстановлением FeBr3 железными
стружками, а также растворы гидроокисей или карбонатов натрия или газообразный
сернистый ангидрид, реагирующий с Б. в присутствии паров
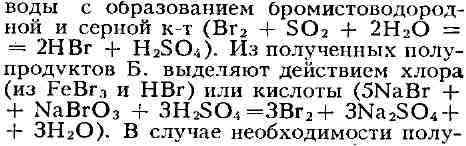
продукты перерабатывают на бромистые соединения, не выделяя элементарного Б.
Вдыхание паров Б. при содержании их в воздухе 1 мг/м3
и более вызывает кашель, насморк, носовое кровотечение, головокружение,
головную боль; при более высоких концентрациях - удушье, бронхит, иногда смерть. Предельно допустимые концентрации паров Б. в воздухе 2 мг/м3.
Жидкий Б. действует на кожу, вызывая плохо заживающие ожоги. Работы с Б.
следует проводить в вытяжных шкафах. При отравлении парами Б. рекомендуется
вдыхать аммиак, используя для этой цели сильно разбавленный раствор его в воде
или в этиловом спирте. Боль в горле, вызванную вдыханием паров Б., устраняют
приёмом внутрь горячего молока. Б., попавший на кожу, смывают большим
количеством воды или сдувают сильной струёй воздуха. Обожжённые места смазывают
ланолином.
Б. применяют довольно широко. Он - исходный продукт для получения ряда
бромистых солей и органич. производных. Большие количества Б. расходуют для
получения бромистого этила и ди-бромэтана - составных частей этиловой жидкости,
добавляемой к бензинам для повышения их детонационной стойкости (см. Антидетонаторы).
Соединения Б. применяют в фотографии, при произ-ве ряда красителей,
бромистый метил и нек-рые другие соединения Б.- как инсектициды. Нек-рые
органич. соединения Б. служат эффективными огнетушаши-ми средствами. Б. и
бромную воду используют при химич. анализах для определения мн. веществ. В
медицине используют бромиды натрия, калия, аммония, а также органич.
соединения Б., к-рые применяют при неврозах, истерии, повышенной
раздражительности, бессоннице, гипертонич. болезни, эпилепсии и хорее.
Лит.: Ксензенко В. И., Стасиневич Д. С., Технология брома и иода, М.,
1960; Позин М. Е.. Технология минеральных солей, 2 изд., Л., 1961; Bromine and
its compounds, ed. Z- E. Jolles, L., 1966. В. К. Бельский, Д. С. Стасиневич.
Бром в организме. Б. - постоянная составная часть тканей животных и
растений. Наземные растения содержат в среднем 7*10-4% Б. на сырое
вещество, животные~1*10-4 %. Б. найден в различных секретах
(слезах, слюне, поте, молоке, желчи). В крови здорового человека
содержание Б. колеблется от 0,11 до 2,00 мг% . С помощью
радиоактивного Б. (82Вr) установлено избирательное поглощение
его щитовидной железой, мозговым слоем почек и гипофизом. Введённые в
организм животных и человека бромиды усиливают концентрацию процессов
торможения в коре головного мозга, содействуют нормализации состояния нервной
системы, пострадавшей от перенапряжения тормозного процесса. Одновременно,
задерживаясь в щитовидной железе, Б. вступает в конкурентные отношения с иодом,
что влияет на деятельность железы, а в связи с этим - и на состояние обмена
веществ.
Лит.: Воинар А. И., Биологическая роль микроэлементов в организме
животных и человека, 2 изд., М., 1960; Верховская И. Н., Бром в животном
организме и механизм его действия, М., 1962.
В. В. Ковальский,
БРОМАТЫ, соли бромноватой кислоты, напр. КВrОз.
БРОМБЕНЗИЛЦИАНИД, бесцветное органическое вещество, C6H5CHBrCN;
tпл 25,40С, плотность 1516 кг/м3
(при 200С), плохо растворим в воде, хорошо - в органических
растворителях. Б. устойчив к действию воды и окислителей; разлагается при
нагревании выше 1200С, а также при действии ряда металлов, к-рые при
этом интенсивно кор-родируют; быстро реагирует со спиртовым раствором
сернистого натрия, что можно использовать для разложения Б. Получают Б.
действием цианистого натрия или цианистого калия на хлористый бензил с
последующим бромированием образующегося при этом цианистого бензила. Б. сильно
действует на слизистые оболочки глаз, вызывая их раздражение и сильное
слезотечение; предложен как слезоточивое отравляющее вещество в конце 1-й
мировой войны.
БРОМБУТИЛКАУЧУК, продукт бромирования бутилкаучука.
БРОМЕЛИЕВЫЕ, ананасные (Вrоmeliaceae), семейство однодольных, б. ч.
травянистых многолетних растений. Ок. 50 родов и до 2000 видов,
распространённых в тропич. и субтропич. Америке. Стебли, как правило,
укороченные, с розетками длинных, часто шиповатых по краям и пёстрых листьев; у
основания они обычно сильно расширены и, плотно охватывая друг друга, образуют
водосборные воронки. Соцветия - колосья, кисти, головки, метёлки, у мн. Б. с
ярко-окрашенными кроющими листьями. Цветки правильные, обоеполые, б. ч.
яркоокрашенные, с трёхчленными чашечкой и венчиком. Тычинок 6, пестик 1
с трёхгнёздной завязью; плод - коробочка или ягода. Лишь немногие Б. растут
на почве, остальные - эпифиты. В воронко-видных розетках листьев Б. скапливаются
вода, органич. остатки и даже фауна и флора; отсюда листья своими основаниями
всасывают воду и питат. вещества. У мн. Б. имеется особая водоносная ткань -
спец. волоски для поглощения влаги. Из широко культивируемых растений к Б.
относится ананас. Др. Б. разводят в оранжереях и комнатах из-за красивых
листьев, ярких цветков и продолжительного цветения. К Б. относится также т. н. луизианский
мох, длинные безлистные нитевидные стебли к-рого, свешивающиеся с деревьев,
используются для набивки матрацев, мебели и т. д. Лит.: Тахтаджян
А. Л., Система и филогения цветковых растений, М.- Л., 1966.
БРОМИДЫ, химич. соединения брома с др. элементами. Б. большинства
металлов представляют собой соли бромисто-водородной кислоты (см. Калия
бромид, Натрия бромид, Серебра бромид и др.). Б. неметаллов (напр., СВr4
и SiBr4), а также металлов III и IV групп периодич. системы (напр.,
АlВr3, SnBr4, TiBr4), как правило,
легкоплавкие, легколетучие вещества; нек-рые из них (напр., РВr3 и
ВВr3) - бромангидриды кислот (т. е. при взаимодействии с
водой образуют соответствующие кислоты, см. Галогенангидриды). Б.
получают непосредственным соединением элементов, взаимодействием НВr с
металлами, окислами, гидроокисями, карбонатами и т. д., а также др. методами.
БРОМИДЫ ПРИРОДНЫЕ, группа редких минералов, относящихся к галогенным
соединениям. Известные в природе минералы ограничиваются бромидами серебра,
кристаллизующимися в ку-бич. системе. Структуры относятся к типу каменной соли.
Чистый бромид серебра - минерал бромирит химич. состава AgBr. Теоретич. состав
броми-рита: Ag 57,44%; Вr 42,56%. Другие минералы - эмболит Ag(Cl.Br) и
иодэм-болит (или иодобромит) Ag (Cl, Вr, I) представляют собой
галогенные соединения серебра, где Вг в значит, мере (до 10-14%) замещается
хлором и иодом. Физич. свойства минералов группы очень близки. Б. п. образуют
мелкие, с ярким алмазным блеском кристаллики кубического или октаэдрического
облика, а также зёрна жёлтого и жёлто-зелёного цвета; мягкие, отчасти
пластичные. Тв. по минералогич. шкале 2-2,5; плотность (в кг/м3) от
5660 (эмболит) до 6350 (бромирит). Б. п. встречаются
исключительно в зонах окисления сульфидных серебро-содержащих месторождений,
формирующихся в засушливых пустынных областях. Г. П. Барсанов.
БРОМИЗОВАЛ, бромурал, лекарственный препарат, оказывающий
успокаивающее и снотворное действие. Применяют как снотворное средство;, детям
Б. назначают также при хорее, коклюше.
БРОМИНДИГО, бромзамещённые индиго, кубовые красители ярких
тоиов от красно-фиолетового до зеленовато-синего цвета. Цвет зависит от
количества атомов галогена и их положения в молекуле. Один из красителей класса
Б.-
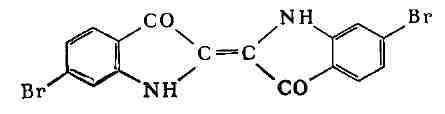
6,6'-диброминдиго - краситель красно-фиолетового цвета, оказался идентичным
"античному пурпуру", применявшемуся для окраски тканей и пряжи за
1400-1500 лет до н. э. и имевшему огромную ценность. Древний пурпур добывали из
раковин пурпурной улитки Ми-rex brandaris (из 12 тыс. улиток можно было
получить 1,4 г красителя).
При бромировании индиго в концентрированной серной к-те или в ледяной
уксусной к-те образуется синий краситель 5,5',7,7'-тетраброминдиго, наз. также
"броминдиго", превосходящий индиго по яркости и устойчивости окрасок
к действию хлора; он широко применяется для окраски хл.-бум. и вискозных
тканей.
Лит.: Коган И. М., Химия красителей, 3 изд., М., 1956. Л. С. Поваров.
БРОМИСТОВОДОРОДНАЯ КИСЛОТА, раствор бромистого водорода в
воде.
БРОМИСТОЕ СЕРЕБРО, AgBr; то же что серебра бромид.
БРОМИСТЫЕ МЕТАЛЛЫ, бромиды, химич. соединения металлов с
бромом; соли бромистоводородной кислоты; см. Бромистый водород.
БРОМИСТЫЙ ВОДОРОД, НВr, соединение брома с водородом; бесцветный газ
с резким запахом и кислым вкусом. tкип-68,70С, (пл - 87,90С.
При 100С в 1 объёме воды растворяется ок. 350 объёмов Б. в. Водный
раствор Б. в. наз. бромистоводородной кислотой. Это бесцветная (иногда
желтоватая из-за присутствия следов брома) жидкость с резким запахом.
При концентрации 47,6% НВr образуется азеотропная смесь, кипящая при
124,30С. Бромистоводородная к-та - одна из самых сильных минеральных
кислот. В пром-сти Б. в. получают взаимодействием паров брома с водородом при
высокой темп-ре. Темп-ру реакции можно понизить катализатором - активированным
углем или платинированным асбестом. В лаборатории Б. в. можно получить
обработкой бромидов 50% -ной серной к-той (более концентрированная кислота
частично окисляет НВr до Вr2) и др. способами. Б. в.
применяют для получения бромидов, органич. бромпроизводных и для др. целей.
БРОМИСТЫЙ КАЛИЙ, КВr, то же, что калия бромид.
БРОМИСТЫЙ НАТРИЙ, NaBr, то же, что натрия бромид.
БРОМЛЕЙ Юлиан Владимирович (р. 21.2.1921, Москва), советский
историк, специалист по ср.-век. истории Хорватии, чл.-корр. АН СССР (1966).
Чл. КПСС с 1944. Окончил ист. ф-т Моск. ун-та (1950). Доктор ист. наук
(1965). В 1952-58 уч. секретарь по координации Отделения истории АН
СССР, в 1958- 1966 уч. секретарь Отделения истории АН СССР. С 1966 директор
Института этнографии АН СССР. С 1968 зам. академика-секретаря Отделения истории
АН СССР. Автор работ "Крестьянское восстание 1573 года в Хорватии"
(1959) и "Становление феодализма в Хорватии" (1964).
БРОМЛИ (Bromley), новый адм. р-н в составе Большого Лондона в
Великобритании. 304,2 тыс. жит. (1968). Пищ., мебельные предприятия;
газовый з-д.
БРОМНАЯ ВОДА, раствор брома в воде. При стоянии на свету
постепенно выделяет О2 в результате разложения присутствующей в ней
НВrО. Б. в. применяют как окислитель и как бронирующее средство - при хим.
анализах и при синтезе нек-рых органич. препаратов.
БРОМНОВАТАЯ КИСЛОТА, НВrОз, неорганич. кислота. В свободном состоянии
не получена, существует в водных растворах с макс, концентрацией 50,6%. На
воздухе при стоянии и особенно при нагревании растворы Б. к. разлагаются. Получают
Б, к. разложением её бариевой соли серной к-той или пропусканием хлора
через бромную воду:
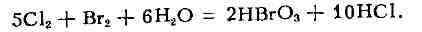
Соли Б. к.- броматы - при обычных условиях устойчивы, а при нагревании
разлагаются с выделением кислорода:
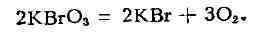
Получаются путём электрохимич. окисления соответствующих бромидов. В кислых
растворах Б. к. и её соли проявляют сильные окислительные свойства,
восстанавливаясь до иона Вr- или до свободного брома; применяются
как окислители.
БРОМНОВАТИСТАЯ КИСЛОТА, НВrО, неорганич. кислота. Существует только в
водных растворах (желтоватая окраска, своеобразный запах), под действием
света разлагается на НВr и кислород; обладает слабыми кислотными свойствами и
является сильным окислителем. Некоторые соли Б. к.- гипобро-миты 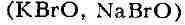 -
получены в свободном состоянии в виде кристаллогидратов. Все они очень
неустойчивы, при нагревании (или подкислении растворов) тотчас
распадаются на бромид и бромат:
-
получены в свободном состоянии в виде кристаллогидратов. Все они очень
неустойчивы, при нагревании (или подкислении растворов) тотчас
распадаются на бромид и бромат: